Опыт использования цетиризина при атопическом дерматите
О.Г. Елисютина, Е.С. Феденко, ГНЦ «Институт иммунологии ФМБА России»;
Российский Аллергологический Журнал № 5–2007, стр. 59–62
Цель. Оценить клиническую эффективность препарата цетиризина дигидрохлорида (Цетрин® «Dr. Reddys Laboratories Ltd.») в комплексной терапии больных атопическим дерматитом (АтД).
Материалы и методы. Под наблюдением находилось 54 больных АтД в возрасте от 18 до 38 лет. Больные АтД были разделены на 3 группы: 1-я группа (n=12) – с тяжелым течением заболевания, 2-я группа (n=34) – со средней степенью тяжести АтД и 3-я группа с легким течением АтД (n=8). Больные принимали препарат по 1 таблетке (10 мг) 1 раз в день независимо от степени выраженности клинических симптомов на момент приема на фоне наружной терапии глюкокортикостероидами, увлажняющими средствами, а также терапии сопутствующих заболеваний. Длительность курса лечения цетиризином составляла 14 дней.
Результаты. На фоне проведенной терапии отмечено достоверное уменьшение индекса SCORAD во всех исследуемых группах. Также отмечено уменьшение индекса кожного зуда и индекса респираторных симптомов. Цетиризин является эффективным антигистаминным средством в комплексном лечении больных АтД.
Введение
Как известно, АтД – аллергическое заболевание кожи, возникающее, как правило, в раннем детском возрасте у лиц с наследственной предрасположенностью к атопическим заболеваниям, имеющее хроническое рецидивирующее течение, возрастные особенности локализации и морфологии очагов воспаления, характеризующееся кожным зудом и обусловленное гиперчувствительностью как к аллергенам, так и к неспецифическим раздражителям. Также АтД сопровождается нарушением сна в той или иной степени, нарушением общего состояния, развитием невротических симптомов, снижением или утратой трудоспособности, социальной дезадаптацией, что в значительной степени влияет на качество жизни [1]. Основным симптомом АтД является кожный зуд. В настоящее время механизм возникновения ощущения кожного зуда остается недостаточно изученным. Важным является тот факт, что нервные окончания, воспринимающие зуд, содержат рецепторы, чувствительные к агентам, вызывающим зуд, например, к гистамину, который является важнейшим посредником аллергического процесса, в том числе при АтД [2]. В процессе аллергического воспаления гистамин высвобождается из тучных клеток и достигает высоких тканевых концентраций. В коже больных АтД содержание гистамина повышено, вместе с тем снижена кожная чувствительность в ответ на аппликацию или внутрикожное введение гистамина. Возможно, при АтД снижена плотность и аффинность Н1-рецепторов или происходит повышенный распад гистамина в коже [3]. Некоторые авторы приписывают именно этим особенностям низкую эффективность некоторых Н1-антигистаминных лекарственных средств (ЛС) у больных АтД. На практике же применение антигистаминных ЛС при АтД клинически оправдано, во-первых, многолетним опытом их успешного применения и, во-вторых, отсутствием альтернативных противозудных средств [3, 4]. Их действие при АтД заключается в конкурентном ингибировании H1 рецепторов, нормализации сосудистого тонуса в коже. Уменьшение периферического сосудистого сопротивления и увеличивающаяся перфузия через пораженные ткани способствуют нормализации метаболических процессов. Таким образом, антигистаминные препараты модифицируют клинический эффект, наблюдаемый в ранней фазе аллергического воспаления [5].
Обоснованием применения антигистаминных ЛС при АтД являются следующие положения:
- участие гистамина в механизме зуда наряду с другими медиаторами;
- наличие сопутствующих респираторных проявлений аллергии, а также профилактика их развития;
- нарушение сна и потребность в седации (Н1 антигистаминные ЛС с седативным эффектом);
Цетиризин является карбоксилированным метаболитом гидроксизина. Данный препарат обладает следующими свойствами:
- высоким сродством к Н1 рецепторам;
- низким уровнем метаболизма;
- наличием дополнительного, возможно, независимого от действия на Н1 рецепторы противоаллергического эффекта;
Это вещество в малой степени связывается с серотониновыми, допаминовыми и адренорецепторами. Цетиризин почти не проникает через гематоэнцефалический барьер. Данные свойства препарата позволяют назначать его больным, для которых даже незначительное угнетение активности ЦНС нежелательно. 70% цетиризина элиминируется почками в неизмененном виде в течение 72 ч. Период полувыведения препарата составляет 10 ч у взрослых и 7 ч у детей, при хронической почечной недостаточности он может увеличиваться до 17 ч. Длительный период выведения позволяет назначать препарат 1 раз в сутки, что позволяет достигнуть комплаентности больного. Цетиризин не ингибирует систему цитохрома Р450. Цетиризин блокирует кожный ответ на фактор, активирующий тромбоциты, важный медиатор хемотаксиса в поздней фазе иммунного ответа и снижает гистохимическое образование морфологического элемента [6].
Цель настоящего исследования заключалась в оценке клинической эффективности и безопасности препарата цетиризина дигидрохлорида на примере Цетрина® (Dr. Reddys Laboratories Ltd.) у больных АтД.
Настоящее исследование проведено на базе отделения аллергии и иммунопатологии кожи ГНЦ «Институт иммунологии ФМБА России».
Материалы и методы
В исследование включено 54 больных АтД в возрасте от 18 до 38 лет. Длительность течения АтД составляла от 2 до 32 лет.
Критерии включения пациентов с АтД в исследование:
- Установленный диагноз АтД в соответствии с критериями Hanifin, Rajka [7]. Тяжесть течения оценивалась в баллах с определением индекса SCORAD (Severity scoring of atopic dermatitis) [8] до и после окончания курса лечения. При величине индекса SCORAD от 0 до 20 течение АтД рассматривалось как легкое, от 20 до 40 баллов – как среднетяжелое, более 40 баллов – как тяжелое;
- Возраст больных от 18 до 50 лет;
- Отсутствие противопоказаний к приему препарата внутрь в соответствии с инструкцией по применению препарата;
- Исключение применения других антигистаминных препаратов в течение периода исследования;
Больные АтД были разделены на 3 группы: 1-я группа (n=12) с тяжелым течением заболевания, 2 -я группа (n=34) со средней степенью тяжести АтД и 3-я группа с легким течением АтД (n=8). Среднее значение индекса SCORAD в 1-й группе до лечения составило 45,5 баллов, во 2-й группе – 34,2, в 3-й группе – 18,9. Отдельно проводилась оценка состояния пациентов по симптому кожного зуда, а также по индексу тяжести респираторных симптомов аллергии. Выраженность этих симптомов оценивалась в баллах от 0 до 3 по следующей шкале: 0 – симптомы отсутствуют, 1 – симптомы выражены слабо, 2 – симптомы выражены умеренно, 3 – симптомы выражены сильно.
Всем больным с АтД было проведено общеклиническое обследование, направленное на выявление сопутствующей патологии и аллергологическое обследование с целью исключения или подтверждения атопии, которое включало в себя определение общего IgE в сыворотке крови, кожные тесты, а также лабораторное определение аллерген-специфических IgE к ингаляционным аллергенам (по показаниям). У 46 больных с АтД были выявлены сопутствующие респираторные проявления атопии – атопическая бронхиальная астма – у 8 больных; аллергический риноконъюнктивит – у 38 больных. У всех пациентов была выявлена сенсибилизация к различным группам аллергенов.
Длительность курса лечения цетиризином составляла 14 дней. Больные принимали препарат по 1 таблетке (10 мг) 1 раз в день независимо от степени выраженности клинических симптомов на момент приема.
Все больные АтД также получали местную базисную терапию: наружные ГКС, увлажняющие средства, а также симптоматическую терапию по поводу выявленной сопутствующей патологии.
Пациенты были инструктированы по алгоритму применения препарата и необходимости проведения самостоятельной оценки самочувствия. За период исследования учитывались симптомы и жалобы пациента до начала лечения, на 7-й день лечения и на 14-й день лечения. Каждый пациент регистрировал динамику симптомов своего заболевания в дневнике самонаблюдения. Врач-исследователь детально оценивал выраженность клинических симптомов и нежелательные явления, определяя их возможную связь с приемом цетиризина.
Всем больным в процессе исследования проводились контрольные анализы крови и другие методы диагностики при необходимости.
Данные фиксировались в амбулаторной или стационарной карте больного. Субъективная оценка состояния сопоставлялась с объективной оценкой врача-исследователя.
Результаты исследования обработаны и сравнены статистически с использованием методов параметрической статистики: проводилось вычисление t критерия Стьюдента для зависимых групп и методов непараметрической статистики – критерий Вилкококсона для парных сравнений с использованием пакета прикладных программ «Statistica 6,0». Различия считались достоверными при р<0,05.
Результаты и обсуждение
Все 54 больных, включенных в исследование, получили полный курс лечения в течение 14 дней. Больные, применявшие цетиризин, отметили значительное уменьшение зуда кожи и воспалительных явлений: на 7-й день лечения значительно уменьшился кожный зуд и количество высыпаний на коже у 36 больных (66,7 от степени тяжести течения АтД, улучшился сон по сравнению с исходным состоянием. На 14-й день лечения положительный эффект отмечен у большинства больных. На рис. 1 и 2 представлена динамика средних значений индекса симптома кожного зуда и индекса SCORAD. Как видно среднее значение индекса SCORAD у больных с тяжелым течением АтД исходно составляло 45,5 баллов, уже через 7 дней лечения его значение снизилось до 36,6 баллов, а через 14 дней зафиксировано уменьшение среднего значения данного индекса до 22,1 баллов. В группе 2 исходное значение индекса SCORAD –34,2, через 7 дней – 26,5, через 14 дней – 17,1. В группе 3 среднее значение индекса SCORAD до лечения составляло 18,9, через 7 дней – 16,4, через 14 дней – 14 баллов.
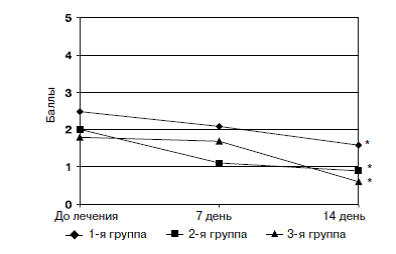
Рис. 1. Динамика тяжести симптомов кожного зуда у больных АтД при применении цетиризина
* различия достоверны по сравнению с оценкой до начала лечения (p<0,05)
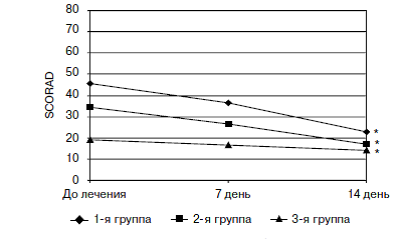
Рис. 2. Динамика индекса SCORAD у больных АтД при применении цетиризина
* различия достоверны по сравнению с оценкой до начала лечения (p<0,05)
При оценке динамики индекса кожного зуда у больных с тяжелым течением АтД (1-я группа) среднее значение данного индекса до включения в схему лечения цетиризина составляло 2,5 баллов, уже через 7 дней отмечено его уменьшение до 2,1 балла, а через 14 дней среднее значение данного показателя уменьшилось и составило 1,6 балла. У больных со средней степенью тяжести АтД (2-я группа) исходное значение данного индекса составляло 2,0 балла, через 7 дней – 1,1 балла, а через 14 дней – 0,9 балла. В 3-й группе значение данного показателя до лечения составляло 1,8 балла, через 7 дней 1,7 балла, через 14 дней – 0,6 балла. Таким образом, уменьшение интенсивности кожного зуда зарегистрировано у большинства больных АтД независимо от степени тяжести заболевания.
При оценке влияния проводимой терапии на проявления сопутствующих респираторных проявлений аллергии показано уменьшение индекса респираторных симптомов аллергии. Его среднее значение в общей группе исследуемых больных АтД с различной степенью тяжести (n=54) до лечения составляло 2,1, через 7 дней 1,8, а через 14 дней отмечено уменьшение среднего значения данного показателя до 1,1 (рис. 3).
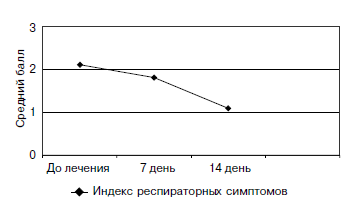
Рис. 3. Динамика индекса сопутствующих респираторных симптомов аллергии в общей группе больных АтД при лечении цетиризином (n=54)
Полученные данные позволяют сделать вывод о достаточной терапевтической эффективности цетиризина на примере Цетрина® при АтД. Препарат эффективно уменьшал зуд, интенсивность высыпаний, а также значительно снижал выраженность сопутствующих респираторных симптомов у больных с АтД.
У 6 больных с АтД, получавших препарат, наблюдался очень слабый седативный эффект, не потребовавший прекращения лечения. У 3 больных с наличием сопутствующей патологии ЖКТ отмечено незначительное появление сухости во рту, чувства тяжести в эпигастрии, но при дальнейшем приеме препарата данные симптомы не возобновлялись. Общее состояние всех больных оставалось удовлетворительным.
Таким образом, применение цетиризина, блокатора Н1-гистаминовых рецепторов 2-го поколения, в комплексном лечении больных с АтД значительно повышает эффективность и сокращает сроки лечения таких пациентов.
Литература
- Российский национальный согласительный документ по атопическому дерматиту. Под ред. Р.М. Хаитова, А.А. Кубановой. Атопический дерматит: рекомендации для практических врачей. М., Фармарус Принт., 2002, 192 с.
- Феденко Е.С. Симптом кожного зуда при атопическом дерматите. Рос. Аллергол. Жур. 2004, № 1, с. 42-47.
- Гущин И.С. Холинергическая система и особенности фармакологического вмешательства в нее некоторых антагонистов Н1-рецепторов. Рос. Аллергол. Жур. 2005, № 6, с. 3-16.
- Dunford P.J, Williams K.N., Desai P.J. Histamine H4 receptor antagonists are superior to traditional antihistamines in the attenuation of experimental pruritus. J. Allergy Clin. Immunol. 2006, v.119, p. 1622-1634.
- Klein P.A., Clark R.A. An evidence_based review of the efficacy of antihistamines in relieving pruritus in atopic dermatitis. Arch. Dermatol. 1999, v. 135, p. 1522-1525.
- Diepgen T.L. Long_term treatment with cetirizine of infants with atopic dermatitis: a multi_country, double_blind, randomized, placebo_controlled trial (the ETAC trial) over 18 months. Pediatr Allergy Immunolog. 2002, v. 13 (4), p. 278-286.
- Hanifin J., Rajka G. Diagnostic features of atopic dermatitis. Acta Derm. Venerol. (Stockh). 1980, v. 114 (Suppl), p. 44-47.
- Stadler J.F., Taieb A. Severity scoring of atopic dermatitis: the SCORAD index. Consensus report of the European task force on atopic dermatitis. Dermatology. 1993, v. 186, p. 23-31.
